Сложные вещества в нашем мире – это разнообразные соединения, которые обладают уникальными свойствами и выполняют важные функции. Эти вещества играют ключевую роль в природных процессах и в жизни организмов, влияют на химические реакции и многое другое. Они организованы из молекул, которые в свою очередь состоят из атомов различных элементов.
Состав сложных веществ может быть очень разнообразным. Некоторые вещества состоят из молекул, состоящих только из одного типа атомов – это простые вещества. Другие вещества имеют сложный состав, включающий в себя различные элементы. Такие соединения называются сложными веществами. Например, вода – это сложное вещество, состоящее из атомов кислорода и водорода.
Свойства сложных веществ определяются их составом и структурой. Различные соединения обладают различными свойствами, такими как цвет, запах, вкус, плотность и т.д. Некоторые вещества обладают высокой степенью устойчивости и стабильности, в то время как другие могут быть очень реактивными и взрывоопасными.
Действие сложных веществ может быть очень разнообразным и зависит от их состава и структуры. Некоторые вещества могут взаимодействовать с другими веществами и вызывать химические реакции. Это может приводить к образованию новых соединений и изменению свойств исходных веществ. Например, соединение между кислородом и горючим веществом может вызвать горение. Другие вещества могут встраиваться в структуру живых организмов и выполнять различные функции, такие как поддержание жизнедеятельности клеток или обеспечение питания организма.
- Вещества и их состав
- Химические элементы и их роль
- Соединения веществ и их разнообразие
- Сложные вещества и их структура
- Атомы и молекулы в сложных веществах
- Органические и неорганические сложные вещества
- Конформация и изомерия в структуре сложных веществ
- Физические свойства сложных веществ
- Плотность и объем сложных веществ
- Температура плавления и кипения
- Электрические и магнитные свойства
- Химические свойства сложных веществ
- Реакционная способность сложных веществ
- Окислительно-восстановительные реакции
- Кислотно-основные свойства
- Фармакологические свойства сложных веществ
- Биодоступность и метаболизм
- 📽️ Видео
Видео:7 класс. Простые и сложные вещества. Формулы: индексы и коэффициентыСкачать

Вещества и их состав
Простые вещества состоят из одного типа атомов. Например, кислород (O) или серебро (Ag) — это простые вещества.
Сложные вещества состоят из разных типов атомов или молекул. Например, вода (H2O) состоит из атомов водорода (H) и атома кислорода (O).
Вещества могут иметь различные физические и химические свойства. Например, они могут быть твердыми, жидкими или газообразными, иметь определенную плотность, температуру плавления и кипения, химическую активность и т.д.
Состав вещества определяется его химической формулой, которая показывает, из каких атомов или молекул оно состоит. Например, формула H2O показывает, что вода состоит из двух атомов водорода и одного атома кислорода.
Знание состава и свойств веществ позволяет нам лучше понять их поведение и использование в различных областях, таких как химия, физика, медицина и технологии.
Химические элементы и их роль
Элементы разделены на различные классы в зависимости от их физических и химических свойств. Некоторые элементы, такие как кислород, водород и углерод, являются основными для органической химии. Они входят в состав всех органических соединений, включая жизненно важные молекулы, такие как белки, углеводы и жиры.
Другие элементы, такие как железо, кальций и магний, играют важную роль в биологических процессах. Они являются необходимыми компонентами для работы многих ферментов и гормонов.
Технические элементы, такие как алюминий, золото и серебро, имеют широкое применение в промышленности. Они используются для производства различных материалов, от конструкций до электроники.
Каждый элемент имеет свою уникальную роль в природе и обществе. Изучение свойств и взаимодействий элементов позволяет развивать новые материалы, лекарства и технологии, что способствует прогрессу человечества.
Соединения веществ и их разнообразие
Вещества могут образовывать разнообразные соединения, такие как соли, оксиды, кислоты, основания, органические соединения и многое другое. Соли образуются в результате реакции кислоты и основания, при которой происходит обмен протонами. Оксиды — это соединения, состоящие из кислорода и другого элемента, которые могут быть как ионными, так и ковалентными. Кислоты и основания являются соединениями, которые проявляют кислотные и основные свойства соответственно.
Органические соединения — это соединения, содержащие углерод, которые образуют основу органической химии. Они могут иметь различные структуры, состоящие из атомов углерода и других элементов. Органические соединения могут быть простыми, такими как углеводы, жиры и белки, а также сложными, например, лекарственные препараты и пластические материалы.
Разнообразие соединений веществ обусловлено большим количеством элементов, которые могут соединяться друг с другом, а также разными способами соединения. Каждый элемент имеет свои характеристики, которые могут влиять на свойства соединения.
Для лучшего понимания разнообразия соединений веществ была разработана таблица Менделеева, которая классифицирует элементы по атомному номеру и химическим свойствам. Таким образом, можно предсказать, какие соединения могут образовывать элементы и какие свойства этих соединений будут иметь.
| Название соединения | Описание |
|---|---|
| Соли | Образуются в результате реакции кислоты и основания. Имеют ионное строение. |
| Оксиды | Соединения, состоящие из кислорода и другого элемента. Могут быть ионными или ковалентными. |
| Кислоты | Проявляют кислотные свойства. |
| Основания | Проявляют основные свойства. |
| Органические соединения | Соединения, содержащие углерод. Имеют разнообразные структуры и могут быть простыми или сложными. |
Соединения веществ представляют собой удивительное разнообразие и имеют важное значение в нашей жизни. Они составляют основу для многих химических реакций и процессов, а также используются в различных областях, включая медицину, промышленность и сельское хозяйство.
Видео:Химические свойства металлов. 9 класс.Скачать
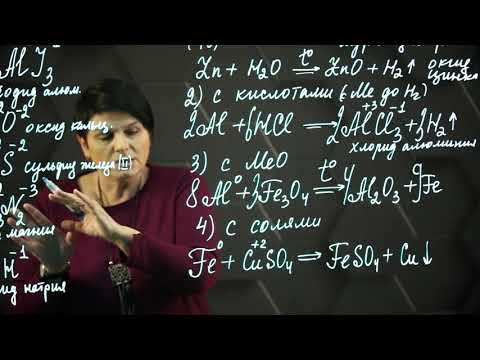
Сложные вещества и их структура
Сложные вещества представляют собой материалы, образованные из более простых веществ, которые объединены в определенной структуре. Эта структура определяет свойства и действие этих сложных веществ.
В основе структуры сложных веществ лежит молекулярная компонента, состоящая из атомов. Атомы связаны между собой с помощью химических связей. Эти химические связи могут быть различного типа и обладать разной прочностью.
Сложные вещества могут содержать одинаковые или разные молекулы, которые образуют структурные блоки. Эти блоки также связаны между собой и образуют более крупные образования. Такие структуры могут быть очень разнообразными и варьироваться в размере и форме.
Свойства сложных веществ зависят от их структуры. Например, некоторые вещества могут быть твердыми, жидкими или газообразными при комнатной температуре в зависимости от структуры и молекулярной компоненты. Также структура может определять растворимость вещества, его химическую активность и способность проводить электрический ток.
Исследование структуры сложных веществ имеет огромное значение для разработки новых материалов с уникальными свойствами. Понимание структуры позволяет контролировать и изменять свойства материалов, что является основой для создания новых технологий и применений.
Таким образом, структура сложных веществ играет важную роль в понимании и использовании этих веществ. Изучение структуры открывает новые возможности для развития науки, технологий и прогресса человечества в целом.
Атомы и молекулы в сложных веществах
Протоны заряжены положительно, нейтроны не имеют заряда, а электроны заряжены отрицательно. Протоны и нейтроны находятся в атомном ядре, а электроны движутся вокруг ядра по орбитам.
Молекулы состоят из двух или более атомов, которые связаны между собой химическими связями. Химические связи возникают, когда атомы обменивают или делают совместное использование своих электронов. Это обмен или совместное использование электронов позволяет атомам образовывать стабильные молекулы.
Молекулы в сложных веществах могут быть очень разнообразными. Они могут состоять из одного типа атомов (например, кислорода в воздухе) или из различных типов атомов (например, вода, состоящая из атомов кислорода и водорода).
Свойства сложных веществ определяются не только типами и количеством атомов или молекул в них, но и химическими связями между этими атомами или молекулами. Химические связи могут быть ковалентными (с общим использованием электронов), ионными (передача или приобретение электронов) или водородными (слабые связи, образованные водородным атомом).
Сложные вещества могут обладать различными физическими и химическими свойствами, такими как температура плавления и кипения, растворимость, электропроводность и т. д. Эти свойства зависят от состава и структуры сложного вещества.
Исследование атомов и молекул в сложных веществах является основой для понимания их свойств и применений в различных областях науки и техники. Познание состава и действия сложных веществ позволяет разрабатывать новые материалы, лекарственные препараты, катализаторы и многое другое.
Органические и неорганические сложные вещества
Сложные вещества могут быть разделены на две основные категории: органические и неорганические. Органические вещества состоят из углерода в связи с другими элементами, такими как водород, кислород, азот и другие. Неорганические вещества, напротив, могут быть образованы без присутствия углерода.
Органические вещества широко распространены в живой природе и являются основой органической химии. Они включают в себя такие классы веществ, как углеводороды, аминокислоты, жиры, белки и др. Органические соединения имеют сложные структуры, состоящие из взаимосвязанных атомов, образующих цепочки, кольца и другие формы. Они обладают химическими свойствами, такими как способность к реакциям с другими веществами, образование новых соединений и т.д.
Неорганические вещества, напротив, в основном образуются в неживой природе и включают в себя множество соединений, таких как соли, оксиды, гидроксиды и др. Неорганические соединения имеют более простую структуру, чем органические, и часто образуют кристаллические сетки. Они тоже обладают химическими свойствами, такими как растворимость в воде, реактивность с другими веществами и т.д.
Важно отметить, что границы между органическими и неорганическими веществами не всегда четко определены. Например, существуют органические соединения, содержащие некоторые неорганические элементы, а также неорганические соединения, содержащие углерод в небольшом количестве. Тем не менее, обычно органические и неорганические соединения характеризуются различными свойствами и образуют различные классы веществ, которые изучаются в химии и других науках.
Конформация и изомерия в структуре сложных веществ
Конформация — это различные пространственные формы, которые может принимать молекула сложного вещества в результате вращения атомов вокруг своих связей. Конформационная изменчивость может проявляться в виде различных конформеров, которые могут иметь различные свойства и активность. Конформация может влиять на физические и химические свойства вещества, его растворимость, стабильность, реакционную способность и биологическую активность.
Изомерия — это явление, при котором вещества имеют одинаковую химическую формулу, но различную структуру и свойства. Изомеры могут отличаться расположением атомов в пространстве или последовательностью связей между атомами. Изомерия может приводить к различной активности и эффективности вещества. Например, в биологически активных веществах изомеры могут иметь различную фармакологическую активность, токсичность и степень воздействия на организм.
Конформация и изомерия являются важными аспектами изучения сложных веществ. Понимание их структуры и свойств позволяет лучше понять механизмы действия веществ и разрабатывать новые препараты, материалы и технологии.
Видео:ОКСИДЫ, КИСЛОТЫ, СОЛИ И ОСНОВАНИЯ ХИМИЯ 8 класс / Подготовка к ЕГЭ по Химии - INTENSIVСкачать

Физические свойства сложных веществ
Сложные вещества имеют разнообразные физические свойства, которые определяют их природу и характеристики. Все сложные вещества обладают определенной структурой и состоят из атомов, молекул или ионов.
Одно из основных физических свойств сложных веществ — температура плавления и кипения. Эти значения зависят от межатомных или межмолекулярных взаимодействий. Например, металлы имеют высокую температуру плавления, так как их атомы образуют кристаллическую решетку, которая требует большого количества энергии для разрыва связей.
Еще одно физическое свойство — плотность. Плотность сложных веществ указывает на их массу в единицу объема. Например, свинец имеет высокую плотность, так как его атомы плотно упакованы и занимают маленький объем.
Теплоемкость — это еще одно важное физическое свойство сложных веществ. Теплоемкость показывает количество теплоты, которое необходимо передать веществу для изменения его температуры. Различные вещества имеют разную теплоемкость, что определяет их способность поглощать и отдавать тепло.
Оптические свойства также важны при изучении сложных веществ. Некоторые вещества пропускают свет, некоторые отражают его, а некоторые поглощают. Эти свойства зависят от электронной структуры вещества.
Электрические свойства сложных веществ определяют их проводимость электричества. Некоторые вещества являются хорошими проводниками, например, металлы, так как у них есть свободные электроны, которые могут передавать электрический заряд. Другие вещества, такие как полупроводники и диэлектрики, имеют разную проводимость в зависимости от внешних условий.
В общем, физические свойства сложных веществ определяют их поведение и взаимодействие с окружающей средой. Изучение этих свойств позволяет понять структуру и состав сложных веществ, а также предсказать их возможные применения в различных областях науки и техники.
Плотность и объем сложных веществ
Объем — это мера пространства, занимаемого веществом. Он может зависеть от температуры и давления, поэтому для физических расчетов часто используются стандартные условия.
Плотность сложных веществ играет важную роль в различных областях науки и техники. Например, она может быть использована для определения концентрации вещества в растворе или для расчета массы материала, необходимого для изготовления определенного изделия.
Плотность может быть выражена различными единицами измерения, такими как г/см³, кг/м³ или фунт/кубический фут. Для удобства расчетов, в науке и технике, часто используется система Международных единиц (СИ), где плотность измеряется в килограммах на кубический метр (кг/м³).
Вычисление плотности сложных веществ обычно основано на знании их состава и массы каждого компонента. Для этого может использоваться формула: плотность = масса / объем. Зная плотность вещества, можно также рассчитать его объем или массу при известных значениях других параметров.
Важно отметить, что плотность сложных веществ может меняться в зависимости от условий, таких как температура и давление. Поэтому при проведении экспериментов и расчетов необходимо принимать во внимание эти факторы.
Изучение плотности и объема сложных веществ имеет большое значение для понимания их свойств и применения в различных областях науки и техники.
Температура плавления и кипения
Температура плавления зависит от ряда факторов, таких как давление, влияние примесей или растворителей, а также химический состав вещества. Например, некоторые металлы имеют очень высокую температуру плавления, такие как вольфрам (3422 °C), в то время как некоторые органические соединения имеют низкую температуру плавления, например, бензол (5,5 °C).
Температура кипения – это температура, при которой жидкое вещество переходит в газообразное состояние. Как и температура плавления, температура кипения зависит от давления и состава вещества.
Некоторые вещества имеют очень низкую температуру кипения, например, водород (−252,87 °C), в то время как другие имеют очень высокую, например, вольфрам (5560 °C). Температура кипения может быть использована для технических и бытовых целей, таких как приготовление пищи, производство лекарств и многих других процессов.
Электрические и магнитные свойства
Сложные вещества обладают разнообразными электрическими и магнитными свойствами, которые определяют их поведение и взаимодействие со средой.
Электрические свойства включают в себя проводимость, диэлектрическую проницаемость и электропроводность вещества. Проводимость определяет способность вещества проводить электрический ток, а электропроводность характеризует степень подвижности свободных зарядов. Диэлектрическая проницаемость отражает способность вещества создавать электрическое поле или изменять его.
Магнитные свойства вещества связаны с его влиянием на магнитное поле. Магнитная проницаемость, коэрцитивная сила и намагниченность являются основными характеристиками магнитных свойств. Магнитная проницаемость определяет способность вещества пропускать магнитные силовые линии. Коэрцитивная сила характеризует силу поля, необходимую для размагничивания вещества, а намагниченность отражает степень намагниченности вещества под воздействием внешнего магнитного поля.
Для более полного изучения электрических и магнитных свойств сложных веществ используется методика их измерения с помощью специальных приборов и аппаратов.
| Свойство | Описание |
|---|---|
| Проводимость | Способность вещества проводить электрический ток |
| Электропроводность | Степень подвижности свободных зарядов |
| Диэлектрическая проницаемость | Способность вещества создавать или изменять электрическое поле |
| Магнитная проницаемость | Способность вещества пропускать магнитные силовые линии |
| Коэрцитивная сила | Сила поля, необходимая для размагничивания вещества |
| Намагниченность | Степень намагниченности вещества под воздействием внешнего магнитного поля |
Видео:ВСЕ химические свойства сложных веществ с нуля! | Вадим Едемский | Химия ОГЭСкачать

Химические свойства сложных веществ
Сложные вещества обладают разнообразными химическими свойствами, которые определяются их составом и структурой. Химические реакции сложных веществ могут быть разнообразными и включать в себя процессы, такие как окисление, восстановление, синтез, разложение и др.
Одно из важных химических свойств сложных веществ — их способность взаимодействовать с другими веществами. Это взаимодействие может приводить к образованию новых соединений, изменению состояния вещества или образованию осадка. Например, некоторые сложные вещества могут реагировать с кислородом из воздуха и окисляться, что приводит к изменению их цвета или структуры.
Другое важное химическое свойство сложных веществ — их растворимость. Растворимость определяет способность вещества растворяться в определенном растворителе. Некоторые сложные вещества могут полностью растворяться в воде, образуя прозрачные растворы, в то время как другие вещества могут быть практически нерастворимыми в воде и образовывать осадок.
| Химическое свойство | Описание |
|---|---|
| Окисление | Процесс, при котором вещество теряет электроны и образуются окислитель и восстановитель. |
| Восстановление | Процесс, при котором вещество приобретает электроны и образуется восстановленное соединение. |
| Синтез | Процесс, при котором из простых веществ образуется сложное соединение. |
| Разложение | Процесс, при котором сложное вещество распадается на простые вещества. |
Химические свойства сложных веществ могут быть исследованы с помощью различных химических реакций и аналитических методов. Понимание этих свойств позволяет углубленно изучать и применять сложные вещества в различных отраслях науки и промышленности.
Реакционная способность сложных веществ
Сложные вещества обладают различной реакционной способностью, которая определяется их структурой и составом. Реакционная способность сложных веществ возникает в результате взаимодействия их атомов, ионов или молекул с другими веществами.
Способность сложных веществ проявлять реакции может быть различной. Некоторые вещества проявляют свойства кислот или оснований и реагируют с другими веществами, образуя соли. Другие вещества могут быть окислителями или восстановителями и участвовать в окислительно-восстановительных реакциях. Есть также вещества, которые могут образовывать комплексы с металлами или обладать хелатообразующими свойствами.
Реакционная способность сложных веществ зависит от их электронной структуры и наличия свободных электронных пар. Вещества с неполностью заполненными энергетическими оболочками более активны и легче участвуют в химических реакциях. Одновременно, реакционная способность может также зависеть от степени окисления атомов в молекуле и их взаимодействия с окружающими ионами или молекулами.
- Реакционная способность сложных веществ может проявляться в возникновении гомолитических или гетеролитических разрывов химических связей, образовании новых связей или обмене ионами.
- Некоторые сложные вещества могут подвергаться полимеризации, поликонденсации или полиаддиции, образуя полимерные структуры.
- Реакционная способность сложных веществ может также проявляться в образовании комплексных соединений или координационных соединений с металлами.
- Некоторые сложные вещества могут образовывать осажденные вещества при реакции с растворами или при выпадении из газообразной фазы.
Реакционная способность сложных веществ является важной характеристикой, которая позволяет оценить их возможности в химических превращениях и использовании в различных процессах. Изучение реакционной способности сложных веществ позволяет расширить наши знания о химии и разработать новые материалы и технологии.
Окислительно-восстановительные реакции
Окислительно-восстановительные реакции основаны на понятии окисления и восстановления. Окисление — это процесс, в котором вещество теряет электроны, а восстановление — наоборот, процесс приобретения электронов. Комбинация окисления и восстановления образует окислительно-восстановительную реакцию.
ОВР встречаются повсеместно в нашей повседневной жизни и играют важную роль в различных отраслях промышленности. Например, эти реакции используются в процессе производства электроэнергии, производстве стали, производстве пластмасс и т.д.
Окислительно-восстановительные реакции могут быть разделены на несколько типов:
- Окислительные реакции — вещество окисляется и теряет электроны;
- Восстановительные реакции — вещество восстанавливается и приобретает электроны;
- Каталитические реакции — электроны передаются через катализатор;
- Индуктивные реакции — электроны передаются между связанными атомами внутри молекулы.
Для проведения окислительно-восстановительных реакций часто используются специальные вещества, называемые окислителями и восстановителями. Окислитель — это вещество, которое способно получать электроны, а восстановитель — вещество, способное отдавать электроны.
Овладение основами окислительно-восстановительных реакций поможет лучше понимать процессы, происходящие в окружающем нас мире, и в дальнейшем может быть полезно в различных химических и промышленных приложениях.
Кислотно-основные свойства
Вещества могут обладать кислотно-основными свойствами, которые определяются их способностью выделять или принимать протоны (H+). Кислотно-основные свойства играют важную роль в различных областях науки и повседневной жизни.
Кислоты являются веществами, которые способны выделять протоны при реакции. Они образуют ионизированные частицы, содержащие положительно заряженные атомы водорода. Примерами кислот являются соляная кислота (HCl), уксусная кислота (CH3COOH) и серная кислота (H2SO4).
Основания, напротив, принимают протоны. Они содержат отрицательно заряженные группы атомов, которые могут привлекать протоны из других веществ. Примерами оснований являются гидроксид натрия (NaOH), гидроксид аммония (NH4OH) и гидроксид калия (KOH).
Кислотно-основные свойства веществ определяют их реактивность и способность участвовать в химических процессах. Например, кислоты и основания могут реагировать друг с другом, образуя соль и воду. Этот процесс называется нейтрализацией. Нейтрализационные реакции широко применяются в лаборатории и промышленности.
Кислотно-основные свойства также играют важную роль в биологии. Многие жизненно важные процессы в организмах связаны с уровнем кислотности и щелочности. Например, желудочный сок обладает кислотными свойствами, необходимыми для пищеварения. Кровь и другие телесные жидкости имеют строго установленный показатель pH, который регулирует множество биологических процессов.
- Кислотно-основные свойства веществ важны для понимания многих явлений в естествознании и химии.
- Кислоты и основания могут реагировать друг с другом, образуя соль и воду.
- Нейтрализационные реакции широко применяются в лаборатории и промышленности.
- Уровень кислотности и щелочности имеет важное значение для многих биологических процессов.
Видео:Простые и сложные веществаСкачать

Фармакологические свойства сложных веществ
Сложные вещества обладают разнообразными фармакологическими свойствами, которые определяют их влияние на организм человека. За счет уникальной комбинации химических соединений, сложные вещества могут производить различные фармакологические эффекты.
| Свойство | Описание |
|---|---|
| Анальгезирующее | Сложные вещества могут обладать способностью снижать боль и облегчать дискомфорт, что делает их эффективными в лечении различных болевых симптомов. |
| Противовоспалительное | Некоторые сложные вещества обладают способностью снижать воспаление в организме, что может быть полезным в лечении заболеваний, связанных с воспалительными процессами. |
| Антибиотическое | Определенные сложные вещества обладают способностью уничтожать или замедлять рост бактерий, что делает их эффективными в лечении инфекционных заболеваний. |
| Антигистаминное | Сложные вещества могут препятствовать действию гистамина — вещества, ответственного за аллергические реакции организма, что делает их эффективными в лечении аллергических заболеваний. |
| Противоопухолевое | Некоторые сложные вещества способны замедлять рост опухолей или уничтожать раковые клетки, что делает их потенциально полезными в лечении онкологических заболеваний. |
Это лишь небольшой перечень фармакологических свойств сложных веществ. Благодаря своим уникальным химическим свойствам, сложные вещества представляют огромный потенциал для разработки новых лекарственных препаратов и терапевтических методов.
Биодоступность и метаболизм
Метаболизм – это совокупность химических реакций и превращений, которые происходят в организме для обработки и использования веществ. Метаболизм включает в себя абсорбцию, распределение, обмен и выделение веществ.
При взаимодействии с организмом, сложные вещества проходят различные стадии биодоступности и метаболизма. Сначала вещество поступает в организм через рот, кожу или другие пути. Затем оно попадает в желудок или кишечник, где может происходить его разложение и усвоение.
Организм может обрабатывать вещество различными путями. Например, ферменты в желудке и кишечнике могут расщеплять сложные молекулы на более простые. Затем вещество может попасть в кровь, где его можно распределить по тканям и органам для дальнейшего использования.
Однако не все вещества полностью усваиваются организмом. Некоторые могут претерпевать метаболические изменения, превращаясь в другие вещества, которые могут быть более или менее активными их исходных форм. Такие изменения могут оказывать влияние на эффективность и безопасность вещества.
Биодоступность и метаболизм могут оказывать значительное влияние на фармакологические и токсические свойства сложных веществ. Изучение этих процессов помогает лучше понять, как вещества взаимодействуют с организмом и какая доза может быть эффективной и безопасной.
📽️ Видео
Атомы и молекулы. Простые и сложные вещества. 7 класс.Скачать

Химия 8 Простые и сложные вещества Состав веществСкачать
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ХИМИЯ 8 класс // Подготовка к ЕГЭ по Химии - INTENSIVСкачать

Как строить структурные формулы быстро, как ФЛЭШ — Мое полное РуководствоСкачать

ЛЕКЦИЯ 1.2. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ. КИСЛОТНОСТЬ-ОСНОВНОСТЬСкачать
Все классы в неорганике за 6 часов | Химия ЕГЭ 2023 | УмскулСкачать

13. Простые вещества (металлы и неметаллы)Скачать

Сложные вещества. Урок 8. Химия 7 класс.Скачать

Классификация неорганических веществ для ОГЭСкачать

Химические свойства веществ. Общие представления.Скачать

14. Строение веществ (простых и сложных)Скачать

Простое вещество и химический элемент. В чем разницаСкачать

Подготовка к ОГЭ. Выпуск № 11 "Химические свойства простых и сложных веществ"Скачать

Занятие 6 | Сложные вещества. Химические формулы веществ | Курс химии | 7 классСкачать

Составление уравнений химических реакций. 1 часть. 8 класс.Скачать
