Аккумуляторные батареи — это источники постоянного тока, которые используются в различных устройствах и системах для обеспечения энергией. Они состоят из нескольких основных компонентов, каждый из которых выполняет свою роль в структуре и принципе работы батареи.
Одним из ключевых компонентов аккумуляторной батареи является электролит. Электролит — это вещество, способное проводить электрический ток. Он разделяет два электрода, положительный и отрицательный, и позволяет передвижение ионов из одного электрода в другой.
Другим важным компонентом является анод, который представляет собой положительный электрод. В аккумуляторной батарее он обычно изготовлен из металлического материала, такого как свинец или кадмий. Анод отвечает за отдачу электронов во внешнюю среду и является местом окисления в ходе работы батареи.
Катод — это отрицательный электрод в аккумуляторной батарее. Он обычно состоит из материала, способного принимать электроны, например, графита или лития. Катод является местом восстановления электронов и основой для образования ионов. Он также выполняет роль вторичного регистра, чтобы ионы могли перемещаться между электродами во время работы батареи.
Принцип работы аккумуляторной батареи основан на химической реакции, происходящей при зарядке и разрядке. Во время зарядки, электрический ток протекает через аккумулятор, приводя к окислению анода и восстановлению катода. При разрядке, химическая реакция происходит в обратном направлении, обеспечивая выход электрического тока внешней среде.
Таким образом, понимание структуры и принципа работы аккумуляторной батареи является важным для эффективного использования и управления ею. Батареи являются неотъемлемой частью нашей повседневной жизни, поэтому важно знать, как эти устройства работают и как правильно ухаживать за ними, чтобы продлить их срок службы.
Видео:КАК УСТРОЕН АККУМУЛЯТОР АКБСкачать
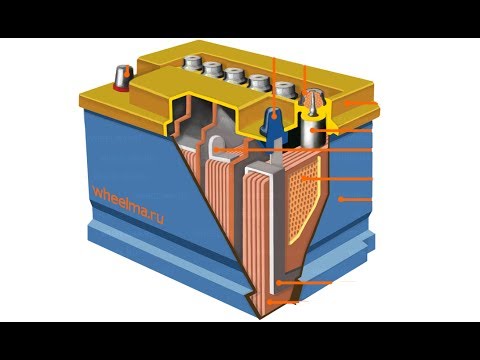
Аккумуляторная батарея: что это такое?
Основными компонентами аккумуляторной батареи являются:
- Анод – электрод, на котором происходит окислительная реакция, освобождающая электроны;
- Катод – электрод, на котором происходит восстановительная реакция, принимающая электрические электроны;
- Электролит – вещество, обеспечивающее передачу ионов между анодом и катодом;
- Сепаратор – преграда, предотвращающая прямой контакт анода и катода и непосредственное короткое замыкание.
Принцип работы аккумуляторной батареи основан на электрохимической реакции между компонентами. Во время зарядки, электрическая энергия, подаваемая на батарею, приводит к протеканию обратной реакции окисления-восстановления. В этот момент происходит его накопление. Когда батарею подключают к потребителю, происходит прямая реакция окисления-восстановления, в результате которой выделяется электрическая энергия, которая используется в качестве источника питания. Таким образом, аккумуляторная батарея позволяет многократно накапливать и использовать электрическую энергию без необходимости постоянной замены источника питания.
Аккумуляторные батареи широко используются в различных областях, включая электромобили, беспроводные устройства, портативную электронику и даже солнечные энергосистемы.
Видео:Устройство и принцип работы автомобильного аккумулятора. Схема аккумулятора.Скачать

Основные компоненты аккумуляторной батареи:
Аккумуляторная батарея состоит из нескольких основных компонентов, каждый из которых выполняет свою функцию и влияет на общую работу и производительность батареи.
Основные компоненты аккумуляторной батареи включают:
| Компонент | Описание |
|---|---|
| 1. Анод | Это положительный электрод, который принимает электроны во время процесса разряда аккумулятора. |
| 2. Катод | Это отрицательный электрод, которые отдаёт электроны во время процесса разряда аккумулятора. Катод также является местом химических реакций, происходящих внутри батареи. |
| 3. Электролит | Это вещество, которое позволяет ионам свободно перемещаться между анодом и катодом. Он является проводником электричества в батарее. |
| 4. Сепаратор | Это материал, разделяющий анод и катод батареи. Сепаратор предотвращает прямое контактирование электродов, защищая батарею от короткого замыкания. |
| 5. Оболочка | Это внешний покров батареи, обычно сделанный из металла или пластика, который защищает компоненты батареи от внешних факторов и предотвращает утечку электролита. |
Все эти компоненты работают вместе, чтобы обеспечить хранение и отдачу энергии в аккумуляторной батарее. Их правильная работа и взаимодействие является ключевым для долговечности и эффективности батареи.
Электролит
В аккумуляторных батареях наиболее распространенным типом электролита является растворная соль или электролит с жидкой или гелевой консистенцией. Растворимые соли, такие как сульфат аммония или серная кислота, обеспечивают проводимость ионов, необходимую для процесса зарядки и разрядки батареи.
Электролит также должен обладать минимальным сопротивлением, чтобы эффективно перемещать заряженные ионы между электродами. Он должен быть стабильным и химически инертным, чтобы не привести к разрушению аккумулятора.
| Типы электролитов | Описание |
|---|---|
| Гелевый электролит | Густая гелевая смесь, образованная полимерами и электролитическими растворами |
| Жидкий электролит | Жидкое вещество, часто на основе растворимых солей или кислот |
| Твердый электролит | Твердое вещество, обладающее ионной проводимостью, например, литий-ионные полимеры |
Выбор электролита в аккумуляторной батарее зависит от требований по емкости, стоимости, безопасности и других факторов. Например, литий-ионные батареи обычно используют жидкий электролит, так как он обеспечивает высокую энергоемкость и энергетическую плотность.
В целом, электролит является ключевым компонентом аккумуляторной батареи, обеспечивая эффективное и надежное функционирование всей системы.
Анод
При заряде аккумулятора на аноде происходит окисление, а при разряде — восстановление. Анод изготавливается из материалов, обладающих высокой окислительной активностью, таких как свинец или свинцовые сплавы.
Окисление, происходящее на аноде, обусловлено действием положительного электрического потенциала, служащего для притяжения отрицательно заряженных ионов. В результате окисления на аноде образуется положительно заряженный ион. При процессе разряда батареи наоборот, на аноде происходит восстановление положительно заряженного ионна за счет отрицательного электрического потенциала.
Катод
Главная функция катода – взаимодействие с анионами, или отрицательными ионами, которые перемещаются от анода к катоду во время разряда аккумулятора. Катод играет ключевую роль в процессе обмена электронами и ионами между активными материалами. Он принимает электроны от внешней цепи, одновременно освобождая ионы и нейтральные частицы, которые являются продуктами электрохимических реакций. Кроме того, катод также обеспечивает защиту активных материалов от окисления.
В зависимости от типа аккумуляторной батареи, катод может быть выполнен из различных материалов. Например, в свинцово-кислотных аккумуляторах катод обычно состоит из свинца или свинцового оксида. В литий-ионных аккумуляторах в качестве катода используются окиси лития или лионометаллоксиды. Катоды никель-кадмиевых аккумуляторов, в свою очередь, изготавливаются из окисей никеля.
Катод является одним из ключевых элементов аккумуляторных батарей. Его способность взаимодействовать с ионами позволяет аккумулировать и хранить электрическую энергию, а также обеспечивает стабильное и эффективное функционирование аккумуляторов.
Видео:Как работает батарейка?Скачать

Принцип работы аккумуляторной батареи:
Принцип работы аккумуляторной батареи основан на электрохимической реакции между анодом и катодом через электролит. Во время зарядки аккумулятора, электрический ток приводит к окислению материала анода, что приводит к выделению электронов.
Одновременно с этим, происходит редукция материала катода, который принимает эти электроны и реагирует с ионами в электролите. В результате этих химических реакций аккумуляторная батарея накапливает электрическую энергию.
При разрядке аккумулятора, электрический ток протекает в обратном направлении, вызывая химическую реакцию в противоположном направлении. Анод и катод меняются местами, и электрическая энергия превращается в электрический ток, который можно использовать для питания различных устройств.
Важно отметить, что химический состав и структура аккумуляторной батареи могут отличаться в зависимости от ее типа, такого как свинцово-кислотный аккумулятор, литий-ионный аккумулятор или никель-кадмиевый аккумулятор. Однако, основной принцип работы остается неизменным — хранение и высвобождение электрической энергии через электрохимические реакции.
Зарядный процесс
В батареи применяется принцип электрохимической реакции, основой которой является окислительно-восстановительная реакция. Во время зарядки активная материя анода теряет электроны, а катода получает их. Это связано с перемещением ионов через электролит, который разделяет электроды. Электроны проходят по внешней цепи, создавая электрический ток.
Зарядный процесс может быть осуществлен с помощью различных источников энергии. Наиболее часто используемыми методами являются зарядка от сети переменного тока или от солнечных панелей. Однако необходимо придерживаться определенных правил зарядки, чтобы предотвратить перегрев аккумулятора и его долговечность.
Важно отметить, что некоторые типы аккумуляторных батарей имеют свои особенности зарядного процесса. Например, для литий-ионных аккумуляторов используется специальная система управления зарядом, которая контролирует напряжение и ток зарядки.
В общем, зарядный процесс является неотъемлемой частью работы аккумуляторной батареи. Благодаря этому этапу батарея получает энергию для своей работы и может быть повторно использована после разряда.
Разрядный процесс
Когда аккумуляторная батарея используется, разрядный процесс начинается. При разрядке, химическая энергия, хранящаяся в активном материале одного из электродов, превращается в электрическую энергию.
Во время разрядного процесса электролит, находящийся между электродами, действует как проводник для передачи электрического заряда. Энергия, полученная из активного материала одного из электродов, переходит через электролит и поступает на второй электрод.
В результате этого процесса происходит отсчет времени работы батареи. Постепенно активный материал разряжается, а заряд электрода снижается. Аккумуляторная батарея будет полностью разряжена, когда все активные материалы обоих электродов будут преобразованы в другие соединения и потеряют свою энергию.
После полной разрядки батареи, ее можно заново зарядить через соответствующий источник электрической энергии, чтобы восстановить активные материалы электродов и вернуть батарее свою емкость.
💡 Видео
ЗА № 31: УСТРОЙСТВО АВТОМОБИЛЬНОГО АККУМУЛЯТОРА. И принцип работы.Скачать

Устройство аккумулятораСкачать

Как работает литий-ионная батарея?Скачать

ЧТО ВНУТРИ БАТАРЕЙКИ и как она работает? ▶️ Часть 1 | COMFYСкачать

Как устроен аккумулятор автомобиляСкачать

Общее устройство легкового автомобиля в 3D. Как работает автомобиль?Скачать

Устройство аккумулятора автомобиля. Tubor EFBСкачать

Виды аккумуляторов. Разбираемся в тонкостяхСкачать

Кислотная аккумуляторная батарея. Устройство, принцип работы и методы диагностикиСкачать
Как устроена батарея ноутбука. Общее устройство батареи и подробное устройство контроллера BMSСкачать

Химические процессы, происходящие в аккумуляторах. 10 класс.Скачать

Как работает батарейка (гальванический элемент)Скачать

БатарейкиСкачать

Из Чего НА САМОМ ДЕЛЕ ДЕЛАЮТ Литий - Ионные Аккумуляторы?Скачать

Тяговый аккумулятор - что это?Скачать

Что внутри аккумуляторных батарей METABO, BOSCH, DEWALT, MAKITAСкачать

Принцип работы генератора переменного токаСкачать
